従来の医療では「不治」と診断されていた難病に、完治の可能性が出てきた。医療の世界におけるイノベーションとして期待されるのが、iPS細胞を使った再生医療である。2014年には世界で初めて、iPS細胞から作製した組織を使った網膜再生の手術が成功した。 そして今、大学などの研究機関ではさまざまな疾病に対する再生医療の研究が加速している。再生医療普及に向けた次の課題は、iPS細胞を基に、狙い通りの細胞を安定した品質で量産すること。そのために京都大学、大日本住友製薬株式会社(以下、大日本住友製薬)、日立の3者によるオープンイノベーションで「大量自動培養装置」の研究開発が急ピッチで進められている。
京都大学の山中伸弥教授が、iPS細胞(Induced Pluripotent Stem Cell:人工多能性幹細胞)を作製してから約10年が経ち、医療への応用が進もうとしている。iPS細胞は、皮膚などの細胞から人工的につくられる多能性幹細胞の一種で、他のあらゆる細胞に分化できる上、分裂を繰り返してほぼ無限に増殖可能という大きな特徴を備えている。従って病気やケガにより失われた細胞を、iPS細胞を基に必要な量だけつくり出して細胞移植をすれば、治癒の可能性が出てくるのだ。
このiPS細胞を使った再生医療が、研究段階を経て実用化のフェーズに移行しつつある。再生医療により神経変性疾患の一種、パーキンソン病治療の研究に取り組むのが、京都大学iPS細胞研究所(CiRA)の髙橋淳教授だ。パーキンソン病は、脳の神経伝達物質であるドパミンを出す神経細胞が減ることで発症する。従来、この病気に対しては対症療法しかなく、薬などにより症状の若干の改善はできても、根治は不可能だった。研究の進捗状況について、髙橋教授が語る。
「iPS細胞からドパミンを出す神経細胞を作製し、患者さんの脳に移植すれば根本的な治療となる可能性があります。2017年に人のiPS細胞からつくった神経細胞をパーキンソン病モデルのサルに移植したところ、手足の震えなどの症状が軽減しました。この研究成果を踏まえて、2018年度中にもヒトに対する治験*2を行う予定ですが、そのためには一つ、クリアしなければならない課題があります」
その課題とは、ドパミン産生細胞の大量培養である。治療目的でヒトに移植するためには、10億個単位の細胞が必要だ。安定した品質の細胞を大量培養するためには、熟練者の手技に頼る従来の手法とは根本的に異なる量産法の開発が欠かせない。
研究により、iPS細胞から再生医療に必要な細胞を培養するプロセス自体は、ほぼ確立された。しかし、再生医療を実際の医療現場で普及させるには、細胞を安定供給する必要がある。そこで、従来の手技による培養に代わり、期待がかかるのが自動培養だ。
また、移植の方式においては、これまで患者本人から作製した細胞を個別に増幅・加工する「自家移植」が主流だが、免疫拒絶がないというメリットがある反面、製造単価も高額になるというデメリットがある。一方、健常なドナーの細胞からあらかじめiPS細胞を作製してストックしておき、目的に応じて必要な細胞を作製して移植する「他家移植」にすれば、製造期間の大幅な短縮化とコストの抑制を実現できる。
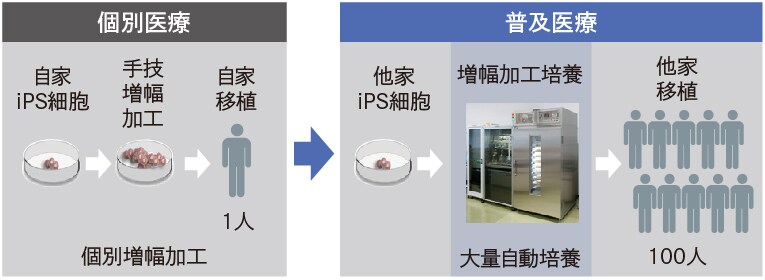
細胞自動培養技術は、手技による培養に比べて製造単価を大幅に低減できる。
この他家移植による「細胞医薬品」製造に取り組むのが、大日本住友製薬である。
「再生医療用の細胞医薬品供給をめざす我々にとっての課題は3つあります。第一が量産する細胞の品質確保、第二が効率的な生産による安定供給、第三が製造コストの低減です」と、同社の取締役 執行役員で、シニアリサーチディレクター兼再生・細胞医薬事業推進担当を務める木村徹氏は語る。
同社は、1990年代から神経細胞を対象とした研究開発を進めてきた。2000年頃から細胞移植による神経再生へと方向を定め、山中教授のiPS細胞創生を受けて、iPS細胞を使った中枢神経の再生に本格的に取り組んでいる。iPS細胞からつくる細胞医薬品は、2030年の中核事業の一つと位置付けられている。
「安定した品質で細胞を量産するには、専用の製造装置の開発が必須。そのパートナーとして、閉鎖系自動培養技術のノウハウを持つ日立への期待は非常に大きい。京都大学の学術的な知見、日立の装置開発の技術力、そして我々の医薬品製造技術を組み合わせたオープンイノベーションによりゴールが見えてきました」(木村氏)

(写真中央)京都大学iPS細胞研究所 臨床応用研究部門 教授 髙橋淳 氏、(写真右)大日本住友製薬 取締役 執行役員 木村徹 氏、(写真左)日立製作所 研究開発グループ 技師長 武田志津
再生医療用の細胞自動培養装置技術の開発については、日立も早くから独自の挑戦を続けてきた。2002年に、東京女子医科大学の岡野光夫教授から寄せられた、細胞培養の自動化というリクエストに応えるため、ロボットを専門とするメカトロニクスのチームが研究開発を開始、後に埼玉県鳩山町の基礎研究センタに場を移して開発を継続している。
「岡野先生のご要望は、カセットに入った細胞を手軽に手術室に持ち込みたいとのことでした。これを実現するため開発されたのが、日立独自の『閉鎖系』自動培養技術です」と、日立神戸ラボ長の武田志津は開発の経緯を語る。
閉鎖系自動培養技術は、従来の手作業やロボットアーム式培養とは根本的に考え方が異なる。これまでのやり方だと、たとえクリーンルーム内とはいえ、人やロボットが作業するためコンタミネーション(生物学的汚染や異物混入)が起こるリスクが比較的高かった。これに対し日立が開発した技術では、外部から完全に閉鎖された無菌空間内で、細胞が自動培養される。

日立独自の閉鎖系自動培養技術は、自動培養および細胞観察を無菌の閉鎖空間で行うことができる。
この技術を基に開発中の大量自動培養装置について髙橋教授は「細胞にとってベストな成長環境で培養できる上、完全に閉鎖された環境の中で精緻なデータを採取できる。人の手では不可能なことを実現した点に、大きな意義があると思います。単に人の作業を機械化しようとしていた従来の技術との決定的な違いですね」と高く評価する。
日立と共同開発中の大量自動培養装置について、木村氏は次のように期待を寄せる。
「自動であり、ヒューマンエラーの入り込む余地がゼロに近い。スタンドアローンのシステムだから、いくらでも、どこにでも必要に応じて増設が可能。これが完成すれば今後、細胞医薬品を事業の一つの柱として考えている我々にとっては、将来を委ねるにふさわしい有望な装置となります」
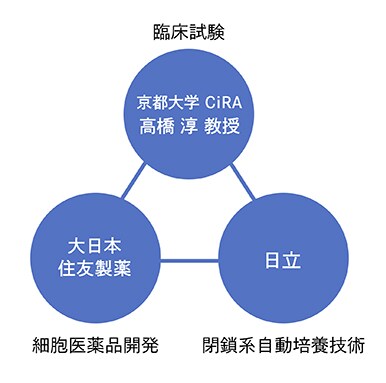
細胞培養の基礎技術を確立し、臨床試験を実施する髙橋教授、細胞医薬品製造に関するノウハウの蓄積を持つ大日本住友製薬、そして細胞量産のための閉鎖系自動培養技術を持つ日立。3者が揃ったことでイノベーションが加速した。その過程を髙橋教授は「みんなが全然違うところから、同じ山の頂上をめざして登っていた。裾野にいる間は、お互いのことはまったくわからないのだけれど、山頂が近づいてくると、当然3者が出会う。そこからみんなで力を合わせて一気に頂上に到達した。そんなダイナミズムを感じました」と振り返る。
2017年に、日立神戸ラボが大日本住友製薬の研究施設である、再生・細胞医薬神戸センターから徒歩10分ほどの場所に新設された。基礎研究センタ(埼玉県鳩山町)からの移転は、現場にどんな変化をもたらしたのだろうか。
「以前なら、ちょっとしたミーティングを開くのにもスーツに着替えて新幹線に乗り、東京まで行かなければならなかった。ところが今はさっと出かけてすぐに会える距離。コミュニケーション密度の高まりは、現場の空気を明らかに変えました」(大日本住友製薬 吉田氏)

(写真右、奥から)大日本住友製薬 再生・細胞医薬神戸センター 吉田賢司 氏、関谷明香 氏、中根淳 氏(写真左、奥から)日立神戸ラボ 加藤美登里、斉藤洸
日立の装置は大日本住友製薬の施設内に設置されており、両社の研究員が同じ部屋の中で実験するケースも多い。何か問題があれば、直ちにその場で話し合って改善策を考え、実行に移す。PDCAサイクルを高速で回しフィードバックを重ねることで、研究開発は加速した。
「同じ装置を前にして、我々は細胞医薬品をつくる立場から、日立は装置開発の立場からの意見をぶつけ合う。お互いに顔を合わせての話なので、本音ベースで遠慮なくものが言える。そのため有益な発見が多く、1回の実験から得られる成果が数倍になったような実感があります」(大日本住友製薬 関谷氏)
日立サイドでの対応もスピードアップした。日立神戸ラボの加藤研究員は「昼間の打ち合わせで受けた指摘を、その日のうちに装置担当と共有し、翌日には改善策を実施して、大日本住友製薬のご担当者に確認してもらう。日々、着実に前進している手応えがあり、技術者としてのモチベーションが高まります」と語る。

日立神戸ラボでの研究風景

動画「日立神戸ラボ 再生医療への取り組み」
髙橋教授は、今回の3者の取り組みについて「早いタイミングから同じ目標に向かい、異なる立場から力を合わせる意義を強く感じました。お互いの考えをダイレクトにぶつけ合いながら研究を進めることで、アカデミアの中に閉じこもっていたときとは異なるダイナミズムが生まれ、研究が深化している実感があります」と評価する。
今回の大量自動培養装置開発において日立は、物理、電気回路、細胞など異なる専門を持つ担当者がチームを組んだ。日立の強みは、必要に応じていつでもバックグラウンドの異なる研究者やエンジニアが集まり、1つのチームを組めること。次に予定されている、細胞の品質検査装置や製造情報の管理システムなどを開発する際には、新たな専門家がチームに加わることになるだろう。将来的には日立独自のAIを活用した解析技術が求められるケースも出てきそうだ。
「我々の使命は、再生医療分野において包括的なソリューションを提供すること。再生医療にとどまることなく、製薬分野での貢献も見据えています」と武田は抱負を語る。
難病に苦しむ患者は日本国内だけでなく、世界中にいる。「日立のグローバルネットワークも活用し、日本発の再生医療を世界に普及させる。そこまでを視野に入れた産学連携のオープンイノベーションは、今後の研究開発の新たなモデルになるのではないでしょうか」と、木村氏は締めくくってくれた。
公開日: 2018年8月
ソリューション担当: 日立製作所 研究開発グループ